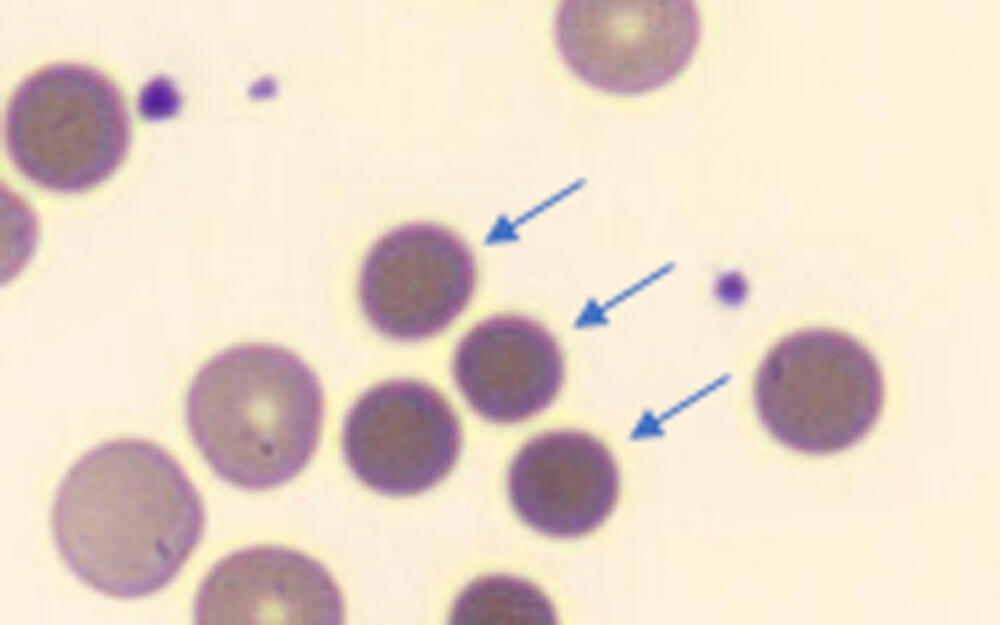
Erfelijke sferocytose (ES) is een frequente oorzaak van chronische hemolytische anemie
20-10-2023
Erfelijke sferocytose (ES) is de meest frequente oorzaak van chronische hemolytische anemie in Noord-Europa. In onze contreien hebben ongeveer 3/10.000 pasgeborenen ES.
Normale rode bloedcellen (RBC) zijn goed vervormbare cellen die daardoor goed doorheen het capillaire vaatbed kunnen circuleren. Deze vervormbaarheid is van essentieel belang voor het normaal functioneren en wordt mogelijk gemaakt door het cytoskelet, dat samengesteld is uit verschillende eiwitten (bv. α- en β-spectrine, ankyrine, band-3).
Bij erfelijke sferocytose komen mutaties voor in de genen die coderen voor deze eiwitten waardoor de morfologie van de RBC beïnvloed wordt. Het klassieke beeld is dat de RBC zich dan als meer rigiede bol- of kogelvormige cellen (met pijltjes aangeduid in onderstaande figuur) gaan presenteren die in het vaatbed van de milt gevangen en afgebroken worden (lyseren). De RBC hebben dan een kortere levensduur dan normaal (±120 dagen). We hebben dus een chronische hemolyse en anemie als gevolg.
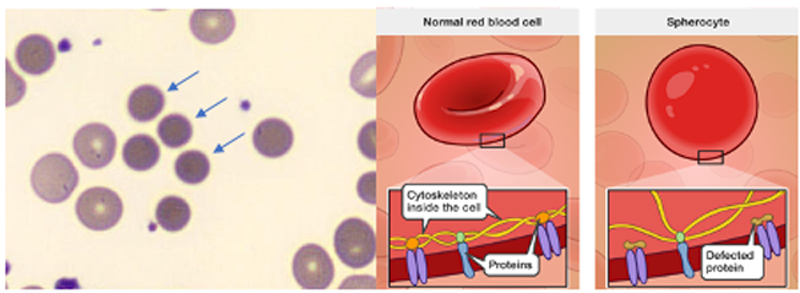
Figuur: Links: microscopisch uitzicht sferocyten (blauwe pijltjes). Rechts: pathofysiologie congenitale sferocytose.
Klinisch voorkomen
De ziekte kan zich al bij de pasgeborene manifesteren, indien niet komt deze meestal op kinderleeftijd tot uiting. Afhankelijk van de mutatie kan de ernst variëren van asymptomatisch tot ernstig, doch meestal zijn de klachten mild. Typische symptomen zijn: (hemolytische) anemie, geelzucht, splenomegalie, en als frequente complicatie galstenen.
Diagnose
Eerste lijn
De diagnose wordt meestal gesteld op basis van een combinatie van de volgende:
- De klinische presentatie (zie hierboven)
- Familiale voorgeschiedenis (in 75% aanwezig). De meeste afwijkingen worden autosomaal dominant overgeërfd, soms autosomaal recessief, maar kunnen ook de novo ontstaan. In dit laatste geval is er dus geen familiale voorgeschiedenis.
- Laboratoriumonderzoeken
- Anemie (gedaald Hb)
- Gestegen mean corpuscular hemoglobin content of MCHC (>33.5 g/dL)
- Een opvallende anisocytose
- In het labo komt dit tot uiting door een gestegen ‘red cell distribution width’ of RDW. Steeds ter beschikking maar wordt niet standaard gerapporteerd.
- Reticulocytose >3% (correleert met de ernst van de hemolyse en de anemie)
- Gestegen indirect bilirubine en gestegen LDH.
- Het onderscheid met immuungemedieerde oorzaken van een (autoimmuun) hemolytische anemie (AIHA) kan gemaakt worden door de negatieve directe Coombs test bij ES.
Tweede-en derdelijn
Soms is de familiale voorgeschiedenis niet duidelijk of blijft er twijfel bij enkele laboparameters en dan moet de diagnose verder uitgewerkt worden. Daarvoor kan men beroep doen op een osmotische resistentietest (de RBC bij ES gaan in vitro sneller lyseren in een hypo-osmotische omgeving). Beter en meer betrouwbaar is de EMA-test (eosine-5-maleimide) analyse op een flowcytometer.
In enkele gespecialiseerde labs kan ook de hoeveelheid spectrine gemeten worden (typisch gedaald bij ES) of kunnen moleculaire analysen helpen bij het opsporen van de moleculaire afwijkingen.
Bij klinisch vermoeden van congenitale sferocytose is het van cruciaal belang om dit te communiceren met het laboratorium. Niet elk bloedstaal wordt namelijk standaard bekeken onder de microscoop!
Differentiaal diagnose
Het onderscheid moet vooral gemaakt worden met aandoeningen die ook een hemolytische anemie veroorzaken. Hierbij onderscheiden we thalassemieën, glucose-6-fosfaat-dehydrogenase deficiëntie (G6PD) en autoimmune hemolytische anemieën (AIHA) .
De AIHA zijn in Vlaanderen de meest voorkomende vormen en kunnen zoals hoger beschreven onderscheiden worden door een directe Coombstest.
Bij hemolytische ziekte van de pasgeborene door maternele antilichamen zal eveneens de directe Coombs test positief zijn.
Behandeling
Bij afwezige of minimale klachten is geen therapie nodig. Bij milde vormen kan extra foliumzuur worden aanbevolen.
Bij ernstige vormen kunnen in acute setting (wissel)transfusies nodig zijn, eventueel aangevuld met EPO. Na verloop van tijd (herhaalde transfusies) kan ijzeropstapeling een probleem vormen, waarvoor ijzerchelatie is aangewezen. Op termijn kan ook een splenectomie overwogen worden om de hemolyse te verminderen (pas vanaf de leeftijd van 7 jaar, en dan ook ondersteund door penicillineprofylaxe en pneumokokkenvaccinatie). Bij galstenen kan een cholecystectomie nodig zijn.
Ten slotte moet men moet erop bedacht zijn dat patiënten met ES gevoeliger zijn voor aplastische crisissen na bv een parvovirus B19-infectie.
